뉴스·공시
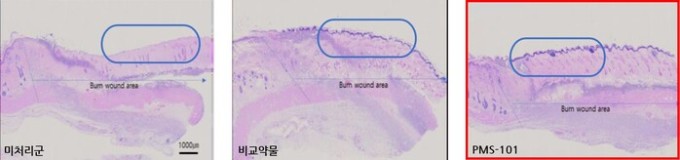 |
| PMS-101 효능 데이터 (사진=강스템바이오텍(217730) 제공) |
[서울 = 뉴스핌] 메디컬투데이 = 강스템바이오텍은 계열사 프리모리스테라퓨틱스의 엑소좀 기반 화상치료제 'PMS-101'이 호주 식품의약품안전청(이하 TGA)으로부터 1/2a상 임상시험계획(CTN)을 승인 받았다고 1일 밝혔다.
호주 CTN은 임상시험 개시를 위한 절차로 국내 임상시험계획(IND)과 동일하게 허가기관으로부터 승인 후 임상시험에 돌입할 수 있다.
PMS-101은 줄기세포 유래 엑소좀 기반 화상치료제다. 엑소좀은 조직재생 및 염증억제 효능이 뛰어나, 손상부위의 염증 반응 후 피부조직이 재생되면서 치유되는 화상 치료에 매우 효과적이다.
프리모리스테라퓨틱스는 하이드로겔 패치 제형으로 화상 부위의 조직재생을 촉진함으로써 현재 화상 표준 치료법인 드레싱 대비 피부가 재건되는(재상피화) 시간을 단축시켰다. 또한, 동물실험을 통해 PMS-101을 사용할 시 새로 성장하는 피부조직의 길이가 약물 미사용군 대비 45%, 현재 치료에 적용되는 약물 대비 23% 증가한다는 데이터를 확보했다.
더불어, 프리모리스테라퓨틱스는 높은 효능의 화상치료제 개발을 위해 기존 엑소좀보다 세포성장, 재생 및 항염 기능을 강화한 엑소좀 'ExoPlus'를 개발했으며, 강스템바이오텍의 CMO(위탁생산)를 통해 100L 스케일에 해당하는 대량생산공정을 구축하여 후기 임상 및 상업화 시 품질관리 등 엑소좀 치료제의 난관 요소인 생산 리스크를 해소했다.
프리모리스테라퓨틱스 나규흠 대표는 "호주 임상시험은 미국의 임상규격을 지켜 수행할 경우 해당 데이터를 인정받아 추후 미국, 유럽 등 글로벌 임상 진행의 토대를 마련할 수 있다. 또한, 국내 시장 점유를 위하여 향후 치료제 개발 시 국내 최대 화상 전문 병원으로의 공급도 협의돼 있다"며 "빠른 상업화를 위해 임상 진입부터 추후 임상 진행방향 및 사업전략 등을 수립한 만큼 이번 임상 1/2a상에서 PMS-101의 안전성과 탐색적 유효성을 확보할 것이다"고 말했다.
이 기사는 메디컬투데이가 제공하는 기사입니다
저작권자(c) 글로벌리더의 지름길 종합뉴스통신사 뉴스핌(Newspim), 무단 전재-재배포 금지
뉴스속보
- 웰스바이오, 일본 검사센터 운영 및 진단 사업 확대 뉴스핌
- 소마젠, NIH로부터 100억원 규모 알츠하이머 유전체 분석 서비스 수주 뉴스핌
- 코로나 백신·진단키트 종목 들썩…실제 매출 수혜주 옥석가리기 한국경제
- [장중수급포착] 엑세스바이오, 외국인 58,941주 대량 순매수... 주가 +8.24% 라씨로
- 프리모리스테라퓨틱스, 엑소좀 기반 화상치료제 호주 임상 1/2a상 IND 승인 뉴스핌
- 강스템바이오텍, 아토피 치료제 두번째 임상 3상 "또 실패"···상업화 멀어지나 뉴스핌
- 소마젠, 美 모더나와 유전체 분석 서비스 공급계약 1년 연장 뉴스핌
- 엑세스바이오, 고민감도 신속진단 기술 "케어슈퍼브" 美 특허 취득 뉴스핌
- 엑세스바이오, 2023년 영업이익 216억 달성…4년 연속 흑자 한국경제
- 웰스바이오, 코로나19 및 독감 동시 진단키트 국내 허가 한국경제





